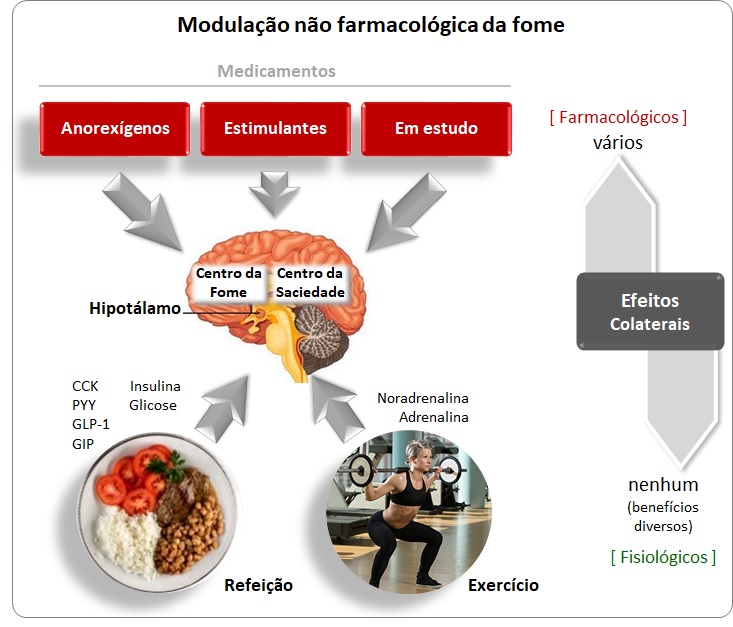
Fome e saciedade são sinais fisiológicos que indicam a necessidade comer e de parar de comer, respectivamente. Apetite é ativado pelos sentidos do olfato, paladar e visão, portanto influenciado por fatores emocionais (desejo) sociais e ambientais. O controle da fome está no hipotálamo, uma estrutura do sistema nervoso que conta com grupos específicos de neurônios com funções de centro de comando da fome e da saciedade. Trata-se de sensações fisiológicas obviamente contrárias, por isso, quando um centro é ativado, o outro e inibido.
CONTROLE DO CONSUMO
Em geral, as sensações de fome e saciedade são muito bem reguladas, porém não funcionam muito bem justamente nas pessoas que mais dependem delas, os sobrepesados e obesos. E a razão é justamente o excesso de peso que, em geral, está associado com o consumo de gorduras saturadas (fontes animais), que causam inflamação e disfunção dos neurônios da saciedade.
CONTROLE FARMACOLÓGICO
Os medicamentos mais utilizados atualmente para emagrecimento (Mounjaro, Zepbound, Ozempic, Wegovy etc) são anorexígenos (inibem centro da fome), fazendo com que o obeso fique sem comer ou coma pouco, sem que represente um grande sacrifício. Alguns usuários relatam que esses medicamentos inibem também a vontade por álcool. Outros medicamentos aceleram o metabolismo e o gasto de energia, tornando ainda mais eficiente o processo.
PROMESSAS ESTUDADAS
O hormônio leptina foi uma promessa em meados da década de 1990 com seu efeito emagrecedor em camundongos (capa das revistas Nature e Science), mas em poucos anos se tornou frustação. A citocina inibitória de macrófagos 1 (MIC-1) despertou o interesse em 2007, quando foi identificada em células tumorais (próstata, mama, pâncreas e colon) como responsável pelo emagrecimento acelerado (anorexia e caquexia) dos pacientes em estágio avançado. Em 2025 a Orforgliprona, uma molécula não-peptídica, agonista do receptor do peptídeo semelhante ao glucagon 1 (GLP-1) passou a ser estuda com resultados até melhores que o Mounjaro e semelhantes.
Exercício físico estimula secreção de adrenalina e noradrenalina, que têm efeito anorexígeno, inibindo a fome no hipotálamo e provocando a termogênese
ANOREXÍGENOS FISIOLÓGICOS
Além dos anorexígenos farmacológicos, a fome pode ser “desligada” simplesmente consumindo alimentos e praticando exercícios. Ao consumir alimentos (de acordo com sua necessidade) o intestino secreta colecistocinina (CCK), peptídeo YY (PYY), peptídeo semelhante ao glucagon 1 (GLP-1) e peptídeo insulinotrópico dependente de glicose (GIP) que, junto com a glicose e insulina, chegam até o hipotálamo e inibem a fome.
POTENTE ANOREXÍGENO E TERMOGÊNICO
Exercício físico estimula as glândulas adrenais a secretarem adrenalina e noradrenalina, os quais têm efeito anorexígeno, inibindo a fome no hipotálamo e provocando a termogênese (acelera o metabolismo). É o mesmo efeito das anfetaminas, que foram prescritas para o emagrecimento durante muitos anos, até a proibição pela Anvisa em 2011. Ao contrário dos medicamentos, os hormônios naturais são secretados em doses exatas, são mais eficientes e livres de efeitos colaterais. Portanto, programe sua dieta e sua prática de exercícios para contar com os efeitos termogênico e modulador da fome dos anorexígenos fisiológicos.
Referências
Comeras LB, Herzog H, Tasan RO. Neuropeptides at the crossroad of fear and hunger: a special focus on neuropeptide Y. Ann New York Acad Sciences. 2019; 1455(1): 59-80. http://dx.doi.org/10.1111/nyas.14179
Milanski M, Degasperi G, Curi R, ..., Saad MJ, Velloso LA. Saturated fatty acids produce an inflammatory response predominantly through the activation of TLR4 signaling in hypothalamus: implications for the pathogenesis of obesity. J Neurosci. 2009; 29(2): 359-70. http://dx.doi.org/10.1523/JNEUROSCI.2760-08.2009
Steinert RE, Feinle-Bisset C, Asarian L, Horowitz M, Beglinger C, Geary N. Ghrelin, CCK, GLP-1, and PYY(3-36): Secretory controls and physiological roles in eating and glycemia in health, obesity, and after RYGB. Physiological Reviews. 2017; 97(1): 411-463. http://dx.doi.org/10.1152/physrev.00031.2014
Stuber GD, Wise RA. Lateral hypothalamic circuits for feeding and reward. Nature Neurosc. 2016; 19: 198-205. http://dx.doi.org/10.1038/nn.4220
Tsai VWW, Husaini Y, Sainsbury A, Brown DA, Breit SN. The MIC-1/GDF15-GFRAL pathway in energy homeostasis: implications for obesity, cachexia, and other associated diseases. Cell Metab. 2018; 28(3): 353-368. http://dx.doi.org/10.1016/j.cmet.2018.07.018
